 物理化学...ppt
物理化学...ppt
《物理化学...ppt》由会员分享,可在线阅读,更多相关《物理化学...ppt(34页珍藏版)》请在第壹文秘上搜索。
1、化学动力学基础化学动力学基础1、化学反应速率、化学反应速率2、化学反应速率的影响因素、化学反应速率的影响因素3、反应机理、反应机理一、反应速率的表示一、反应速率的表示1、平均速率:、平均速率:= c/t2、瞬时速率:、瞬时速率:=dc/dt3、SI单位:单位:mol.m-3.s-1。其他单位如时间用。其他单位如时间用min,h等。常用等。常用单位单位mol.L-1.s-1。二、反应速率的实验测定(二、反应速率的实验测定(c-t曲线)曲线) t /min 0 1 2 3 4 c(N2O5)/molL-1 0.16 0.113 0.080 0.056 0.040 /molL-1min-1 0.05
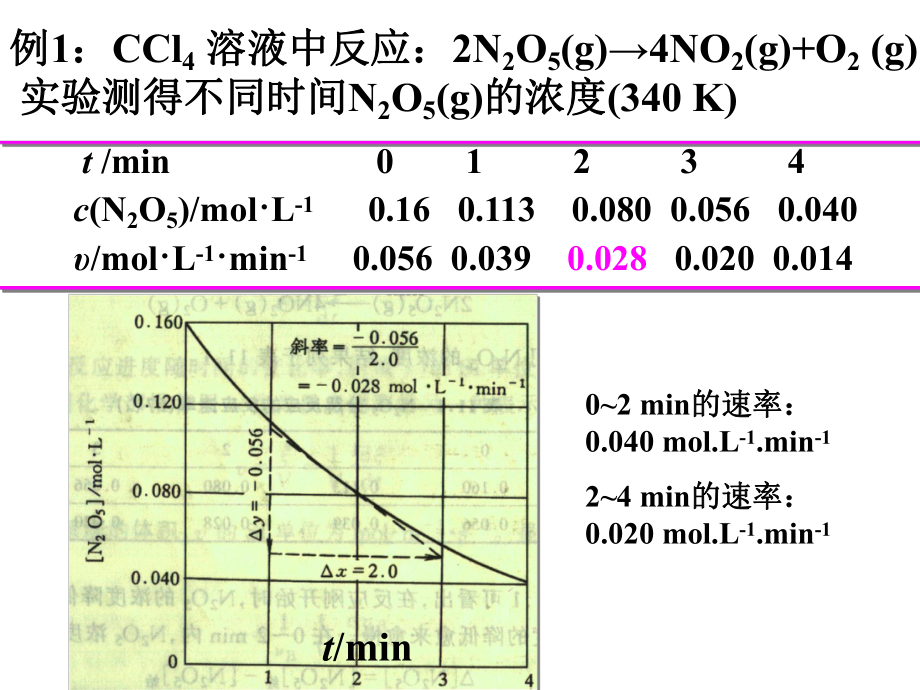
2、6 0.039 0.028 0.020 0.014例例1:CCl4 溶液中反应:溶液中反应:2N2O5(g)4NO2(g)+O2 (g) 实验测得不同时间实验测得不同时间N2O5(g)的浓度的浓度(340 K) t/min 02 min的速率:的速率:0.040 mol.L-1.min-124 min的速率:的速率:0.020 mol.L-1.min-1三、反应速率的影响因素三、反应速率的影响因素1、浓度对反应速率的影响、浓度对反应速率的影响(1)恒温下,基元反应质量作用定律。)恒温下,基元反应质量作用定律。对于一般的化学反应对于一般的化学反应: a A + b B = y Y + z Z =
3、kca(A)cb(B)k为速率常数为速率常数(1-1)k与本性有关,与浓度无关。与本性有关,与浓度无关。(1-2)k与温度有关。与温度有关。(1-3)k有单位,取决于(有单位,取决于(a+b)的值。)的值。a+bk的单位的单位0mol.L-1.s-11s-12L.mol-1.s-1n(L.mol-1)n-1.s-1例例1:CCl4 溶液中反应:溶液中反应:2N2O5(g)4NO2(g)+O2 (g) 实验测得不同时间实验测得不同时间N2O5(g)的浓度的浓度(340 K) t /min 0 1 2 3 4 c(N2O5)/molL-1 0.16 0.113 0.080 0.056 0.040
4、/molL-1min-1 0.056 0.039 0.028 0.020 0.014说明:说明:N2O5(g)的浓度增加一倍,反应速率也增加一倍。的浓度增加一倍,反应速率也增加一倍。一级反应:一级反应:=kc(N2O5(g)(2)一级反应的特点)一级反应的特点-dc/dt=k1c积分后:积分后:lnc=-k1t+B(B=lnco)即:即:c=coe-k1t或:或:k1=(1/t)ln(co/c)当当c=(1/2)co时,时,t为半衰期,记为为半衰期,记为t1/2。k1t1/2=ln2=0.693一级反应的三个动力学特征:一级反应的三个动力学特征:1、k的单位为的单位为时间时间-1。2、lgc对
5、对t作图为一直线,斜率作图为一直线,斜率-k1/2.303,截距,截距lgco。3、半衰期与、半衰期与co无关。无关。例例2:氯乙烷在:氯乙烷在300 K下的分解反应是一级反应,下的分解反应是一级反应,k = 2.510-3 min-1,实验开始时氯乙烷的,实验开始时氯乙烷的c0 =0.40 molL-1,求,求:1、反应进行、反应进行8.0 h,氯乙烷的浓度;,氯乙烷的浓度;2、氯乙烷的浓度降至、氯乙烷的浓度降至0.010 molL-1,反应所需时间。,反应所需时间。3、氯乙烷分解反应的半衰期。、氯乙烷分解反应的半衰期。1、c=coe-kt=0.12 mol.L-12、t=(1/k)ln(c
6、0/c)=1475.55 min=24.6 h3、t1/2=(ln2)/k=277.2 min=4.62 h例例3:30 oC下,下,N2O5在在CCl4中分解为中分解为N2O4和和O2的反应是一级的反应是一级反应,反应,N2O4和和NO2均溶于均溶于CCl4溶液,只有氧气能逸出。用量溶液,只有氧气能逸出。用量气表测定不同时刻逸出气表测定不同时刻逸出O2的体积,如下表所示。求的体积,如下表所示。求N2O5分解分解反应的速率常数和半衰期。反应的速率常数和半衰期。时间时间/min04080120160200240280320O2体积体积/mL015.6527.6537.7048.8552.6758
7、.3063.0066.8584.85一级反应的速率常数与所用浓度无关,可用与浓度成正比的物一级反应的速率常数与所用浓度无关,可用与浓度成正比的物理量代替浓度,理量代替浓度,V即即co,V-V即即c。k=(1/t)ln(co/c),t=40 min, V=15.65 mL, V-V=69.20 mLk=5.1010-3 min-1其他时刻的其他时刻的k分别为分别为4.93、4.90、4.86、4.85、4.84、4.85、4.85均值均值4.9010-3 min-1。t=0.693/(4.9010-3)=141.4 min例例4:在碱性溶液中,次磷酸根离子:在碱性溶液中,次磷酸根离子(H2PO2
8、-)分解为亚磷酸分解为亚磷酸根离子根离子(HPO32-)和氢气,反应式为和氢气,反应式为 H2PO2-(aq)+OH-(aq)=HPO32-(aq)+H2(g)在一定温度下,实验测得下列数据如下:在一定温度下,实验测得下列数据如下:实验编号实验编号cH2PO2-/mol.L-1 cOH-/mol.L-1 /mol.L-1.s-1 1 0.10 0.10 5.3010-9 2 0.50 0.10 2.6710-8 3 0.50 0.40 4.2510-7试求试求 (1)反应级数;反应级数; (2)速率常数)速率常数; (3)当)当cH2PO2- = cOH- = 1.0 mol.L-1时,在时,


- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 物理化学
 第壹文秘所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
第壹文秘所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 重点工作绩效评估自评表.docx
重点工作绩效评估自评表.docx
